SANGUE E DOENÇAS
RESUMO APRESENTAÇÃO DOS COMPONENTES SANGUÍNEOS / AUTOTRANSFUSÃO
A HISTÓRIA DO SANGUE NO MUNDO
A HISTÓRIA DO SANGUE NO BRASIL
Vamos mudar, levar informação fidedignas e fazer parte desta mudança na história? AUTOTRANSFUSÃO
O que é o sangue na realidade?
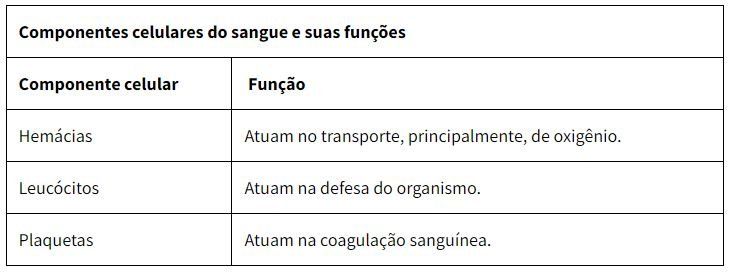
Sabemos que; "O sangue é um tipo especial de tecido conjuntivo que se destaca por apresentar-se como um fluído de cor vermelha e viscoso. Caracteriza-se por apresentar uma matriz líquida (plasma), em que se encontram suspensos os elementos celulares do sangue (hemácias, leucócitos e plaquetas)."
Porém, ele está mais relacionado com RISCO do que benefício o médico precisa levar ao paciente o melhor tratamento e o sangue não é o que existe de melhor, segundo pesquisas mais recentes existem melhores alternativas. pois segundo especialistas a transfusão de sangue traz graves problemas ao paciente. Parece simples mas não é. Injúrias celulares, doenças imunobiológicas e presença de vírus e bactérias. Há falhas e complicações.
Digamos que, o meu sangue é excelente, ele me conhece, conhece meus órgãos, me protege. Ele defende qualquer agressor, qualquer corpo estranho que vier para o meu corpo ele sabe se defender.
Agora, outro sangue em você é um desastre mesmo se HOUVESSE compatibilidade os órgãos de outra pessoa são diferentes dos meus órgãos, com a transfusão o próprio sangue vai combater você mesmo. Antígenos brigando com anticorpos, seu corpo também irá rejeitar o sangue doado porque também não é dele.
Sangue estocado recebe alterações tanto biomecânicas quanto biofísicas.
O sangue estocado na geladeira sofre uma alteração globular. Sua forma normalmente é de disco bicôncava, quando armazenado na geladeira ele se transforma como uma mamona cheio de espiculas , o sangue também endurece (8,0 micrômetros) e provoca dificuldade para a passagem, portanto ele não passa no capilar (4,4 micrometros) obstruindo a Microcirculação. O paciente que faz uso de sangue está relacionado com a morte e insuficiência renal. Efeitos deletérios na estocagem, na manipulação , na própria segurança. É melhor não utilizar o sangue de outra pessoa. Mantenha-se saudável, utilize a AUTOTRANSFUSÃO.
As tecnologias podem resolver esses problemas. A ABA te ajuda.
Entenda mais...
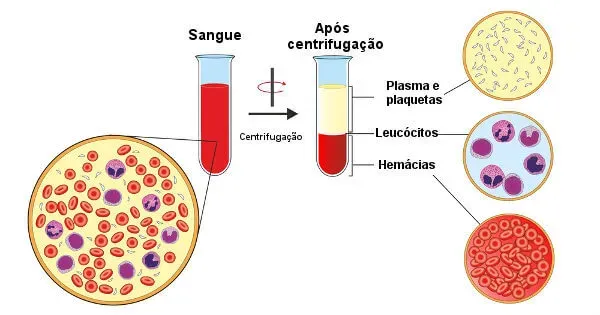
Componentes
O sangue é composto por plasma sanguíneo, dois tipos celulares (eritrócitos e leucócitos) e fragmentos celulares nomeados plaquetas. Os eritrócitos, leucócitos e plaquetas são chamados elementos figurados do sangue. Esses elementos constituem 45% do volume do sangue, enquanto o plasma constitui 55% do seu volume.
Uma pessoa saudável apresenta um volume total de sangue de, aproximadamente, 7% do seu peso corporal.Parágrafo Novo
Plasma sanguíneo
O plasma sanguíneo é a parte líquida do sangue e apresenta-se com uma coloração amarelo-claro. Esse representa mais da metade do volume total de sangue do nosso corpo e é 90% constituído de água.
No plasma são encontrados ainda sais minerais, proteínas, hormônios, entre outras substâncias, como nutrientes e resíduos do metabolismo. É no plasma que estão suspensos os elementos figurados.
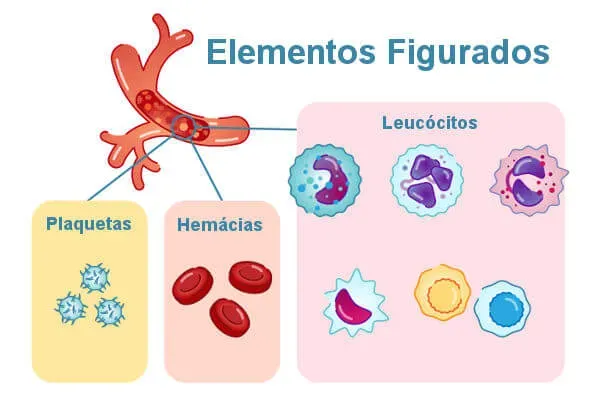
Hemácias, glóbulos vermelhos ou eritrócitos
As hemácias, também conhecidas como glóbulos vermelhos e eritrócitos, são as células responsáveis pelo transporte de oxigênio no organismo. Elas são células anucleadas, ou seja, não possuem núcleo e têm o formato de um disco bicôncavo. Essas células são pequenas, apresentando cerca de sete a oito micrômetros de diâmetro.
As hemácias possuem um período de vida curto, o qual dura cerca de 120 dias, sendo posteriormente destruídas, principalmente no baço. Em condições normais, essas células não saem do interior dos vasos sanguíneos.
A coloração vermelha dessas células é decorrente da presença de uma proteína denominada hemoglobina, que, além de garantir a cor, é a responsável pelo transporte de oxigênio no corpo.
A ausência de núcleo nas hemácias favorece o aumento do espaço para a hemoglobina nessas células. Vale salientar que, além da ausência de núcleo, as hemácias também não possuem mitocôndrias.
Quando observamos uma redução no número de hemácias no sangue, temos uma situação conhecida como anemia.
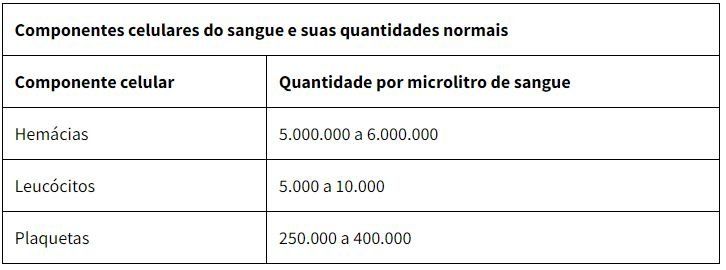
O sangue é vermelho devido à grande quantidade de hemácias encontrada nele. Essa célula é a encontrada em maior quantidade, sendo observados, em cada microlitro de sangue, cerca de cinco a seis milhões de eritrócitos.
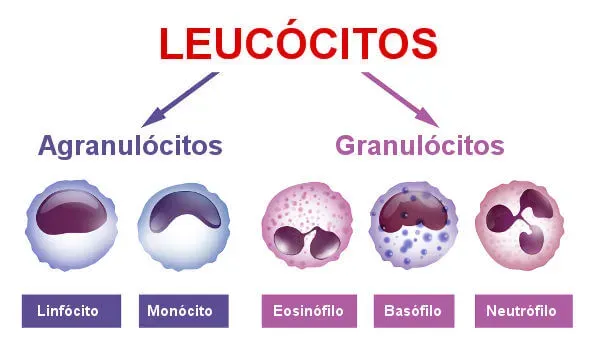
Leucócitos ou glóbulos brancos
Os leucócitos, também chamados glóbulos brancos, são as células responsáveis pela defesa do nosso organismo. São incolores, apresentam formato esférico e são capazes de realizar diapedese, que é sua saída ativa dos vasos sanguíneos, para atuarem na função de defesa em tecidos lesionados ou atacados por agentes patogênicos. Em média, a cada microlitro de sangue, encontra-se de cinco a dez mil leucócitos
Existem diferentes tipos de leucócitos, cada um realizando uma determinada função relacionada com a proteção do corpo. Alguns deles, por exemplo, realizam o processo de fagocitose, outros são responsáveis pela produção de anticorpos, que são proteínas de defesa. Neutrófilos, basófilos, monócitos, eosinófilos e linfócitos são tipos de leucócitos.
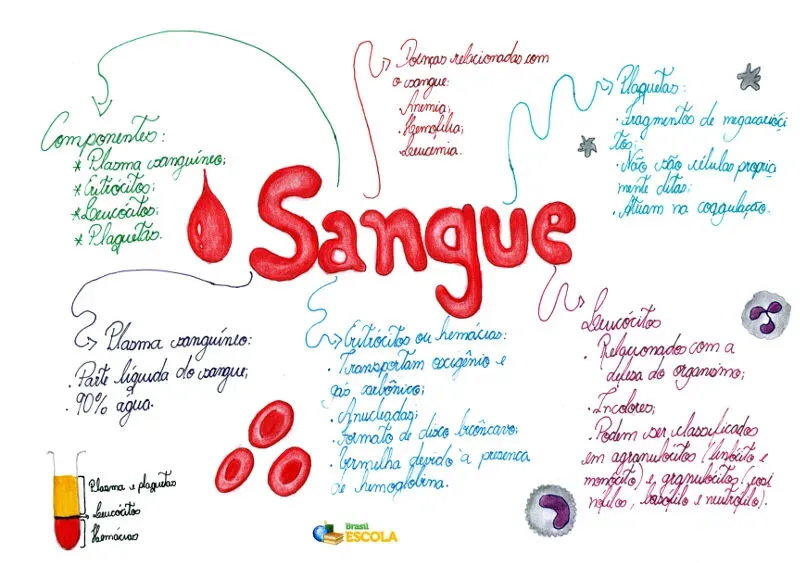
Sangue
O sangue é um tipo especial de tecido conjuntivo relacionado, entre outras funções, com o transporte de nutrientes e gases respiratórios e a defesa do organismo.
O sangue é um tecido conjuntivo com propriedades especiais.
O sangue é um tipo especial de tecido conjuntivo que se destaca por apresentar-se como um fluído de cor vermelha e viscoso. Caracteriza-se por apresentar uma matriz líquida (plasma), em que se encontram suspensos os elementos celulares do sangue (hemácias, leucócitos e plaquetas).
Nos seres humanos, o sangue corre dentro do nosso sistema cardiovascular, o qual é fechado. Isso significa que nosso sangue é encontrado apenas no interior do coração e de nossos vasos sanguíneos.
Geralmente uma pessoa apresenta um volume total de sangue que corresponde a cerca de 7% do seu peso corporal. Com isso, temos que um indivíduo de, aproximadamente, 70 quilos, deve apresentar cerca de cinco litros de sangue.
→ Função
O sangue apresenta diversas funções no corpo, garantindo, por exemplo:
- Transporte de nutrientes;
- Transporte dos gases respiratórios;
- Transporte de resíduos do metabolismo;
- Defesa e imunidade por meio da ação dos leucócitos;
- Coagulação sanguínea por meio da ação das plaquetas.
Em um hemograma, o aumento dos valores de leucócitos pode representar uma infecção.
Os leucócitos são divididos em dois grupos: granulócitos e agranulócitos.
Os granulócitos caracterizam-se por apresentar núcleo com formato irregular e grânulos específicos em seu citoplasma. Neutrófilos, eosinófilos e basófilos são leucócitos do tipo granulócito.
Os agranulócitos, diferentemente do grupo anteriormente citado, apresentam um núcleo com formato mais regular e em seu citoplasma não se observa a presença de grânulos específicos. Linfócitos e monócitos são exemplos de agranulócitos.
Plaquetas
As plaquetas são fragmentos de megacariócitos da medula óssea, ou seja, não são células propriamente ditas. Essas estruturas possuem cerca de dois a três micrômetros de diâmetro e também não possuem núcleo.
Elas atuam no processo de coagulação e também ajudam na reparação de vasos sanguíneos que sofreram algum tipo de lesão. Em cada microlitro de sangue, existem cerca de 150 mil a 450 mil plaquetas.
Em pacientes com dengue, percebe-se uma queda no número de plaquetas. Na dengue clássica, observa-se que essa contagem fica abaixo de 100 mil em cada microlitro de sangue.
Onde é produzido
O sangue é produzido na chamada medula óssea. Essa está localizada nas cavidades dos ossos esponjosos e também no canal medular dos ossos longos.
DOENÇAS TRANSFUSIONAIS
As complicações mais comuns da transfusão são
- Reações não hemolíticas febris
- Reações com calafrios
As complicações mais graves, com taxas de mortalidade muito elevadas, são
- Reação hemolítica aguda (RTHA) por incompatibilidade ABO
- Doença do enxerto-versus-hospedeiro (DEVH)
- Sobrecarga circulatória associada à transfusão
- Lesão pulmonar aguda relacionada com a transfusão (LPART)
Outras complicações incluem
- Reações alérgicas
- Afinidade do oxigênio alterada
- Reação transfusional hemolítica tardia
- Infecções
- Púrpura pós-transfusional
O reconhecimento precoce dos sintomas sugestivos de reação transfusional e a informação imediata ao banco de sangue são essenciais. Os sintomas mais comuns são calafrios, rigidez, febre, dispneia, tontura, urticária, coceira e dor no flanco. Se qualquer um desses sintomas (que não seja urticária e coceira localizada) ocorrer, a transfusão deve ser interrompida imediatamente e o acesso IV mantido pérvio com soro fisiológico normal. Resto do produto do sangue e amostras anticoaguladas e coaguladas do sangue do paciente devem ser enviadas para o banco de sangue para investigação. NOTA: a unidade em questão não deve ser reiniciada e a transfusão de qualquer unidade previamente providenciada não deve ser iniciada. Transfusão adicional deve ser retardada até que a causa da reação seja conhecida, a menos que a necessidade seja urgente, caso em que eritrócitos tipo O Rh negativo devem ser utilizados.
A hemólise do doador ou do receptor (geralmente o primeiro) durante ou após a transfusão pode resultar de incompatibilidade ABO/Rh, anticorpos do plasma ou eritrócitos frágeis ou hemolisados (p. ex., superaquecimento do sangue armazenado ou contato com soluções hipotônicas IV). A hemólise é mais comum e grave quando os doadores de eritrócitos incompatíveis são hemolisados pelos anticorpos do plasma do receptor. As reações hemolíticas podem ser agudas (dentro de 24 h) ou tardias (de 1 a 14 dias).
Reação transfusional não hemolítica febril
Reações febris podem ocorrer sem hemólise. Os anticorpos direcionados contra o antígeno leucocitário humano (HLA) dos leucócitos no sangue de um doador de outra maneira compatível são uma possível causa. Essa causa é a mais comum em pacientes multitransfundidos ou em multíparas. As citocinas liberadas dos leucócitos durante o armazenamento, em particular em concentrados de plaquetas, são outra causa possível.
Clinicamente, as reações febris consistem em aumento da temperatura ≥ 1° C, calafrios e algumas vezes cefaleia e dor dorsal. Os sintomas simultâneos de reação alérgica são comuns. Como a febre e os calafrios também prenunciam a reação transfusional hemolítica grave, todas as reações febris devem ser investigadas, como também todas as reações transfusionais hemolíticas graves.
A maioria das reações febris é tratada, com sucesso, com paracetamol e, se necessário, difenidramina. Os pacientes também devem ser tratados (p. ex., com paracetamol) antes das transfusões futuras. Se o receptor sofreu mais de uma reação febril, filtros especiais de leucorredução são usados para transfusões futuras; muitos hospitais utilizam componentes pré-armazenados leucorreduzidos do sangue.
Reação transfusional hemolítica aguda (RTHA)
Cerca de 20 pessoas morrem todos os anos nos EUA em decorrência de reação transfusional hemolítica aguda. RTHA geralmente resulta da reação dos anticorpos do plasma do receptor contra os eritrócitos do doador. A incompatibilidade de antígenos ABO é a causa mais comum de reação transfusional hemolítica aguda. Os anticorpos contra os antígenos de grupos sanguíneos não ABO também podem ocasionar RTHA. O erro habitual é a ausência de identificação (etiqueta) na amostra pré-transfusional do receptor no momento da coleta e a falha em cruzar a amostra do receptor em questão com o hemocomponente imediatamente antes da transfusão.
A hemólise é intravascular, provocando hemoglobinúria com graus variáveis de insuficiência lesão renal aguda e, possivelmente coagulação intravascular disseminada (CID). A gravidade da reação transfusional hemolítica aguda depende de
- Grau de incompatibilidade
- Quantidade de sangue administrada
- Velocidade de administração
- Integridade dos rins, fígado e coração
A fase aguda normalmente ocorre na 1ª hora do início da transfusão, mas pode ocorrer mais tarde durante a transfusão ou imediatamente depois. O início é muitas vezes abrupto. O paciente pode se queixar de desconforto e ansiedade. Pode haver dispneia, febre, calafrios, rubor facial e dor intensa, em especial na área lombar. Pode haver evolução para choque, com pulso rápido e fraco; pele fria e pegajosa; baixa pressão arterial; e náuseas e vômitos. Icterícia pode se seguir após hemólise aguda.
Se ocorrer RTHA sob anestesia geral, os únicos sintomas podem ser hipotensão, sangramento incontrolável em locais de incisão e nas mucosas provocado por coagulação intravascular disseminada (CIVD) associada, ou urina escura que reflete hemoglobinúria.
Se houver suspeita de RTHA, um dos primeiros passos é verificar de novo a amostra e as identificações do paciente. Confirma-se o diagnóstico por um teste de antiglobulina direta positivo, medição da hemoglobina urinária, desidrogenase láctica (LDH) sérica, bilirrubina e haptoglobina. A hemólise intravascular produz hemoglobina livre no plasma e na urina; os níveis de haptoglobina são muito baixos. Pode ocorrer hiperbilirrubinemia subsequente.
Após a fase aguda, o grau da lesão renal aguda determina o prognóstico. A diurese e a diminuição de ureia sanguínea normalmente necessitam de recuperação. A insuficiência renal permanente não é comum. A oligúria prolongada e o choque são sinais de prognóstico reservado.
Se houver suspeita de RTHA, a transfusão deve ser interrompida e o tratamento de suporte iniciado. A meta da terapia inicial é atingir e manter adequadamente a pressão arterial e o fluxo de sangue renal com soro fisiológico a 0,9% IV e furosemida. O soro fisiológico IV é administrado para manter a eliminação da urina em 100 mL/h por 24 h. A dose inicial de furosemida é de 40 a 80 mg (1 a 2 mg/kg em crianças), com doses futuras ajustadas para manter o fluxo urinário > 100 mL/h no primeiro dia.
O tratamento medicamentoso da hipotensão deve ser feito com cautela. Os fármacos pressóricos, que diminuem o fluxo sanguíneo renal (p. ex., adrenalina, noradrenalina, alta dose de dopamina), são contraindicados. Se o fármaco pressórico é necessário, normalmente dopamina, 2 a 5 mcg/kg/min, é utilizada.
O nefrologista deve ser consultado o quanto antes, em particular se não houver resposta diurética dentro de 2 a 3 h após o início da terapia, o que pode indicar necrose tubular aguda. A terapia adicional de líquido e diuréticos pode ser contraindicada e a diálise precoce pode ser útil.
Doença do enxerto-versus-hospedeiro (DEVH)
A causa da doença do enxerto versus hospedeiro (ver também Rejeição de enxerto e doença do enxerto versus hospedeiro) associada às transfusões normalmente é causada pela transfusão de produtos contendo linfócitos imunocompetentes para um hospedeiro imunocomprometido. Os linfócitos do doador atacam os tecidos do hospedeiro porque o seu sistema imunitário não consegue destruir os linfócitos do doador. A doença enxerto versus hospedeiro pode ocorrer ocasionalmente nos pacientes imunocompetentes se receberem sangue de um doador (muitas vezes um parente próximo) homozigoto para um haplótipo de antígeno leucocitário humano (HLA) para o qual o paciente é heterozigoto. Sinais e sintoms incluem febre, exantema (erupções cutâneas que se disseminam centrifugamente, tornando-se eritroderma com bolhas), vômito, diarreia aquosa e sanguinolenta, linfadenopatia e pancitopenia decorrente de aplasia da medula óssea. Icterícia e níveis elevados de enzimas no fígado também são comuns. A doença enxerto versus hospedeiro ocorre 4 a 30 dias após a transfusão, sendo diagnosticada com base na suspeita clínica e nas biópsias da pele e medula óssea. A DEVH apresenta > 90% de mortalidade, pois não há tratamento específico disponível.
A prevenção de doença enxerto versus hospedeiro é feita com irradiação (para lesar o DNA dos linfócitos doadores) de todos os hemocomponentes transfundidos. Ela é feita
- Se o receptor for imunocomprometido (p. ex., paciente com síndrome de imunodeficiência congênita, neoplasias hematológicas, transplante de células-tronco hematopoiéticas; recém-nascidos)
- Se o sangue do doador for obtido de um parente de 1º grau
- Quando há transfusão de componentes compatíveis com o HLA, excetuando-se as células-tronco
O tratamento com corticoides e outros imunossupressores, incluindo aqueles usados em transplante de órgão sólido, não necessita do uso de irradiação.
Sobrecarga circulatória associada à transfusão
Embora a sobrecarga circulatória associada às transfusões seja sub-reconhecida e subnotificada, foi identificada recentemente como sendo a segunda causa mais comum de morte relacionada com transfusões notificadas à FDA (1). A alta carga osmótica dos hemocomponentes aumenta o volume no espaço intravascular ao long de horas, o que pode causar sobrecarga circulatória associada a transfusões em pacientes suscetíveis (p. ex., com insuficiência renal ou cardíaca). Os eritrócitos devem ser infundidos vagarosamente. Os pacientes devem ser observados e, se ocorrerem sinais de insuficiência cardíaca (p. ex., dispneia, estertores), a transfusão deve ser suspensa e o tratamento para insuficiência cardíaca começado.
O tratamento típico é com um diurético, como furosemida 20 a 40 mg IV. Ocasionalmente, nos pacientes que necessitam maior volume de infusão plasmática para reverter sobrecarga de varfarina, pode-se aplicar dose baixa de furosemida simultaneamente; no entanto, o CCP é a primeira escolha para esses pacientes. Os pacientes em alto risco de sobrecarga circulatória associada a transfusões (p. ex., com insuficiência cardíaca ou insuficiência renal grave) são tratados profilaticamente com um diurético (p. ex., furosemida 20 a 40 mg IV).
Lesão pulmonar aguda relacionada com a transfusão (LPART)
A lesão aguda no pulmão relacionada à transfusão consiste em complicação não frequente causada por anticorpos anti-HLA e/ou antigranulócitos no plasma do doador que aglutina e desgranula os granulócitos do receptor dentro do pulmão. Os sintomas respiratórios agudos se desenvolvem e a radiografia torácica tem padrão característico de edema pulmonar não cardiogênico. Essa complicação é a segunda causa mais comum de morte relacionada com transfusões. A incidência é 1 em 5.000 a 1 em 10.000, mas muitos casos são leves. A lesão de pulmão aguda leve a moderada, relacionada à transfusão, é provavelmente despercebida. A terapia de suporte geral tipicamente causa a recuperação sem sequelas que durem muito. Os diuréticos devem ser evitados. Usar sangue doado por homens reduz o risco dessa reação. Os casos devem ser comunicados ao serviço de hemotransfusão do hospital em onde está sendo feita a transfusão ou ao banco de sangue.
Reações alérgicas
As reações alérgicas para componente desconhecido no sangue do doador são comuns, quase sempre em decorrência de alergênios no plasma do doador, ou, com menos frequência, anticorpos de um doador alérgico. Essas reações são normalmente leves e incluem urticária, edema, tontura ocasional e cefaleia durante ou imediatamente após a transfusão. A febre simultânea é comum. Com menos frequência, podem ocorrer dispneia, respiração ofegante e incontinência, indicando espasmo generalizado da musculatura lisa. Raramente ocorre anafilaxia, sobretudo nos receptores com deficiência de IgA.
Em paciente com história de alergias ou reação alérgica à transfusão, um anti-histamínico pode ser administrado profilaticamente logo antes ou no começo da transfusão (p. ex., 50 mg de difenidramina por via oral ou IV). NOTA: os fármacos nunca devem ser misturados ao sangue.
Se uma reação alérgica ocorrer, interrompe-se a transfusão. Um anti-histamínico (p. ex., 50 mg de difenidramina IV) geralmente controla urticária e prurido leves e a transfusão pode ser retomada. No entanto, uma reação alérgica moderada (urticária generalizada ou broncospasmo leve) também requer hidrocortisona (100 a 200 mg IV) e reação anafilática grave requer tratamento adicional com 0,5 mL de solução de adrenalina 1:1.000 por via subcutânea e soro fisiológico a 0,9% IV juntamente com investigação pelo banco de sangue. Outra transfusão não deve ocorrer até que a investigação esteja completa.
Os pacientes com deficiência grave de IgA grave necessitam de transfusão de eritrócitos lavados, plaquetas lavadas e plasma do doador deficiente em IgA.
Afinidade do oxigênio alterada
O sangue armazenado por > 7 dias apresenta 2,3-difosfoglicerato (DPG) do eritrócito diminuído, e o 2,3-DPG está ausente após > 10 dias. Essa ausência resulta na maior afinidade pelo oxigênio e na liberação mais lenta do oxigênio para os tecidos. Há poucas evidências de que a deficiência de 2,3-DPG seja clinicamente significativa, exceto nas exsanguinotransfusões em recém-nascidos, em pacientes com doença falciforme com dor torácica aguda ou acidente vascular encefálico e em alguns pacientes com insuficiência cardíaca grave. Após a transfusão de eritrócitos, o 2,3-DPG se regenera dentro de 12 a 24 h.
Reação transfusional hemolítica tardia
Ocasionalmente, um paciente sensibilizado a um antígeno eritrocitário apresenta níveis de anticorpos muito baixos e testes pré-transfusão negativos. Após a transfusão com eritrócitos com esse antígeno, resposta primária ou anamnéstica pode ocorrer (normalmente em 1 a 4 semanas) e causar reação hemolítica tardia. A reação transfusional hemolítica tardia geralmente não é tão catastrófica quanto a reação transfusional hemolítica aguda. Os pacientes podem ser assintomáticos ou ter febre leve. Raramente, há sintomas graves. Com frequência, ocorre somente destruição dos eritrócitos transfundidos (com o antígeno), resultando em queda do hematócrito e discreto aumento da desidrogenase láctica e da bilirrubina, com teste de antiglobulina direta positivo. Como a reação transfusional hemolítica tardia é quase sempre leve e autolimitada, muitas vezes não é identificada e o indício clínico pode ser queda inexplicável na hemoglobina para o nível pré-transfusão ocorrendo em 1 ou 2 semanas pós-transfusão. As reações graves são tratadas de modo similar às reações agudas.
Doenças infecciosas
Contaminação bacteriana de concentrados de eritrócitos ocorre raramente, talvez em razão de técnica asséptica inadequada durante a coleta ou bacteremia transitória do doador assintomático. O resfriamento dos eritrócitos costuma limitar o crescimento bacteriano, exceto por microrganismos criofílicos como Yersinia, que pode produzir níveis perigosos de endotoxina.
Todas as bolsas de concentrado de hemácias são examinadas quanto a crescimento bacteriano antes de serem liberadas, que é indicado por uma mudança na cor. Como os concentrados de plaquetas são armazenados à temperatura ambiente, têm potencial maior para crescimento bacteriano e produção de endotoxina se contaminadas. Para minimizar o crescimento, o armazenamento é limitado a 5 dias. O risco de contaminação bacteriana das plaquetas é de 1:2.500. Dessa forma, as plaquetas são rotineiramente testadas para bactérias.
Raramente, a sífilis é transmitida em sangue ou plaquetas frescos. O armazenamento sanguíneo ≥ 96 h em 4 a 10° C mata a espiroqueta. Embora regulamentos federais americanos exijam teste sorológico para sífilis no doador de sangue, doadores infectados são soronegativos no início da doença. Os receptores de unidades infectadas podem desenvolver exantemas secundárias características.
Hepatite pode ocorrer após a transfusão de qualquer produto sanguíneo. O risco tem sido reduzido pela inativação viral mediante tratamento com calor da albumina sérica e proteínas do plasma e pelo uso de fatores concentrados recombinantes. Testes para hepatite são necessários em todos os doadores de sangue (ver tabela Exames de transmissão de doenças infecciosas). O risco estimado de transmissão de hepatite B é de 1:1 milhão; de hepatite C < 1:2 milhões. Como provavelmente sua fase virêmica transitória e doença clínica concomitante impedem a doação de sangue, a hepatite A (hepatite infecciosa) não é uma causa significativa de hepatite associada à transfusão.
A infecção pelo HIV nos EUA é quase inteiramente pelo HIV-1, embora o HIV-2 também preocupe. O teste para anticorpos em ambas as doenças é exigido. Testes de ácido nucleico para antígeno HIV-1, assim como para antígeno p24 em HIV-1, também são necessários. Além disso, os doadores de sangue são questionados sobre comportamentos que possam colocá-los em alto risco de infecção pelo HIV. HIV-0 não tem sido identificado entre os doadores de sangue. O risco estimado de transmissão do HIV por transfusão é 1:1.500.000 a 2.000.000.
Citomegalovírus (CMV) pode ser transmitido por leucócitos no sangue transfundido. Não é transmitido pelo plasma fresco congelado. Em razão de o CMV não causar doença em receptores imunocompetentes, a rotina do teste de anticorpo do sangue do doador não é exigida. Todavia, o CMV pode provocar doença grave ou fatal nos pacientes imunocomprometidos, que devem receber hemoderivados negativos para o CMV, de doadores com sorologia negativa para o vírus ou de sangue com leucodepleção por filtros leucocitários.
O vírus linfotrópico 1 da célula T humana (HTLV-1), que pode causar linfoma-leucemia da célula T em adultos e mielopatia associada ao HTLV-1/paraparesia espástica tropical, promove soroconversão pós-transfusional em alguns receptores. Todos os doadores de sangue são testados para anticorpos contra HTLV-1 e -HTLV-2. O risco estimado de resultados falso-negativos no teste do doador de sangue é de 1:641.000.
A doença de Creutzfeldt-Jakob nunca foi registrada como transmitida por transfusão, mas a prática atual impede doação de uma pessoa que tenha recebido hormônio de crescimento derivado de um ser humano ou transplante de dura-máter, ou com um membro da família com essa doença. A variante da doença de Creutzfeldt-Jakob (vCJD, ou doença da vaca louca) não é transmitida por transfusão de sangue. No entanto, os doadores que ficaram por tempo significativo no Reino Unido e em outras partes da Europa são permanentemente recusados para a doação (ver tabela Algumas razões para adiar ou negar a doação de sangue).
Malária é transmitida facilmente por meio de eritrócitos infectados. Muitos doadores não estão conscientes de que tiveram malária, que pode ser latente e transmissível por 10 a 15 anos. O armazenamento não torna o sangue seguro. Os doadores prospectivos devem ser questionados sobre malária ou se estiveram em região onde a malária é prevalente. Os doadores que tiveram o diagnóstico de malária ou são imigrantes, refugiados, ou cidadãos de países onde a malária é considerada endêmica são recusados por 3 anos; viajantes de países endêmicos são recusados por 1 ano.
Babesiose, doença de Chagas e vírus do Nilo ocidental raramente são transmitidos por transfusão.
Foi notificada a transmissão da infecção pelo zika vírus por hemoderivados no Brasil. Portanto, a FDA determinou a realização de testes para o zika vírus nos EUA e em seus territórios. Em vez do teste para zika, as tecnologias de redução de patógenos aprovadas para as plaquetas e o plasma também poderiam ser usadas; no entanto, seu uso é atualmente muito restrito, e essa tecnologia ainda não está disponível para as hemácias.
Púrpura pós-transfusional
A púrpura pós-transfusional é uma complicação muito rara na qual a contagem de plaquetas cai rapidamente de 4 a 14 dias após a transfusão de concentrado de hemácias, causando trombocitopenia moderada a grave. Quase todas as pacientes são multíparas que normalmente receberam a hemotransfusão durante um procedimento cirúrgico. A etiologia exata não está esclarecida. No entanto, a hipótese mais aceita é a de que a paciente negativa para o antígeno plaquetário humano 1a (HPA1a) produz aloanticorpos por causa da exposição ao antígeno HPA1a do feto durante a gestação. Como os eritrócitos armazenados contêm micropartículas de plaquetas e como a maioria dos doadores (99%) é positiva para HPA1a, as micropartículas das plaquetas do sangue do doador podem deflagrar uma resposta de anticorpos nos pacientes previamente sensibilizados (resposta anamnéstica). Como essas micropartículas das plaquetas se ligam às plaquetas do receptor (e, portanto, revestem-nas com o antígeno HPA1a), os aloanticorpos destroem as plaquetas do receptor, causando trombocitopenia. O distúrbio desaparece espontaneamente à medida que as plaquetas revestidas de antígeno são destruídas.
Os pacientes apresentam púrpura juntamente com sangramento moderado a grave — geralmente no local da cirurgia. As transfusões de plaquetas e hemácias pioram o quadro.
O diagnóstico diferencial geralmente é a trombocitopenia induzida por heparina (TIP), embora a TIP não esteja associada a sangramento. O diagnóstico é feito pela identificação dos anticorpos contra o HPA1a no plasma do paciente e pela ausência do antígeno correspondente nas plaquetas do paciente.
O tratamento é feito com altas doses de imunoglobulinas IV (1 a 2 g/kg) e evitando novas transfusões de plaquetas ou hemácias. Pode-se considerar a plasmaférese nos casos graves e, para pacientes com sangramento grave, pode ser feita transfusão de plaquetas de doadores negativos para HPA1a, se disponível.
Complicações da transfusão maciça
A transfusão maciça é a transfusão de um volume de sangue maior ou igual a uma volemia de sangue em 24 h (p. ex., 10 unidades em adulto de 70 kg). Quando um paciente recebe reposição volêmica convencional com papa de hemácia (coloide) e cristaloides (soro fisiológico ou Ringer lactato) em um volume tão alto, os fatores de coagulação e as plaquetas no plasma são diluídos, causando coagulopatia (coagulopatia dilucional). Essa coagulopatia agrava a coagulopatia por consumo decorrente do próprio trauma grave (resultante da extensa ativação da cascata de coagulação) e leva a uma tríade letal de acidose, hipotermia e sangramento.
Recentemente, foram elaborados protocolos de transfusão maciça nos quais as plaquetas e o plasma fresco congelado são administrados mais cedo na reanimação, antes de haver coagulopatia, em vez de tentar "recuperar o terreno perdido". Demonstrou-se que esses protocolos diminuem a taxa de mortalidade, embora as proporções ideais de hemácias, plasma e plaquetas ainda estejam sendo investigadas. Um estudo recente não mostrou diferença significativa na mortalidade entre administrar uma unidade de plasma e um concentrado de plaquetas a cada 2 unidades de concentrado de hemácias (1:1:2) versus administrar uma unidade de plasma e um concentrado de plaquetas a cada 1 unidade de concentrado de hemácias [1:1:1 (2)].
A hipotermia decorrente da transfusão rápida de grandes quantidades de sangue resfriado pode causar arritmias ou parada cardíaca. A hipotermia é evitada pelo uso de um dispositivo IV com troca de calor que aquece suavemente o sangue. Outros tipos de aquecimento do sangue (p. ex., micro-ondas) são contraindicados em razão de lesão potencial do eritrócito e hemólise.
Os efeitos tóxicos do citrato e do potássio geralmente não são preocupantes, mesmo na transfusão maciça; entretanto, os efeitos tóxicos de ambos podem ser potencializados em caso de hipotermia. Os pacientes com insuficiência hepática podem ter dificuldade para metabolizar o citrato. Pode ocorrer hypocalcemia, mas raramente é necessário tratar (com 10 mL de solução de gliconato de cálcio a 10% IV diluída em 100 mLD5W, administrada durante 10 minutos). Os pacientes com insuficiência renal podem ter aumento dos níveis de potássio se forem transfundidos com sangue armazenado por > 1 semana (o acúmulo de potássio normalmente é insignificante no sangue armazenado por < 1 semana). A hemólise mecânica durante a transfusão pode aumentar os níveis de potássio. Pode ocorrer hipopotassemia cerca de 24 h após a transfusão de eritrócitos senescentes (> 3 semanas), que absorvem potássio.
Referências gerais
- 1. FDA: Fatalities reported to FDA following blood collection and transfusion: Annual Summary for Fiscal Year 2018. Silver Spring, MD, US Food and Drug Administration, 2018.
- 2. Holcomb JB, Tilley BC, Baraniuk S, et al: Transfusion of plasma, platelets, and red blood cells in a 1:1:1 vs a 1:1:2 ratio and mortality in patients with severe trauma: the PROPPR randomized clinical trial. JAMA 313(5):471–482, 2015. doi:10.1001/jama.2015.12
Doenças que afetam o sangue
Algumas doenças afetam diretamente as células sanguíneas, desencadeando uma série de consequências desagradáveis e até mesmo fatais. Vejamos, a seguir, algumas dessas doenças:
Anemia: quando há uma redução da quantidade de hemoglobina no sangue. A anemia pode ser desencadeada, por exemplo, por carência de ferro na alimentação e hemorragias. O indivíduo anêmico apresenta, entre outros sintomas, fraqueza, cansaço, falta de ar e tonturas.
Anemia Falciforme: quando se observa uma alteração nas hemácias, as quais apresentam uma forma de foice. Essa alteração pode desencadear a formação de coágulos que levam à obstrução dos vasos sanguíneos, o que pode gerar danos em certos órgãos. Na anemia falciforme, o indivíduo pode apresentar dores e fadiga.
Hemofilia: é um problema genético, ligado ao cromossomo X, que provoca alterações na coagulação do sangue. Isso significa que pessoas com esse problema podem apresentar excessivo sangramento diante de uma lesão. O tratamento da hemofilia geralmente se baseia na reposição do fator de coagulação que não está presente no paciente.
Leucemia: é um tipo de câncer que afeta os glóbulos brancos e caracteriza-se pela produção de células anormais. Existem, de acordo com o Instituto Nacional de Câncer (Inca), mais de 12 tipos diferentes de leucemia. O tratamento da anemia é variado e pode incluir quimioterapia, radioterapia e também transplante de medula óssea.
Tipos sanguíneos
Sabemos que na espécie humana temos quatro diferentes tipos sanguíneos: tipo A, tipo B, tipo AB e tipo O.
Nas pessoas com sangue tipo A, observa-se a presença de aglutinogênio A nas hemácias, enquanto nas pessoas de sangue tipo B, observa-se a presença de aglutinogênio B. Nas pessoas com sangue tipo AB, observa-se a presença de aglutinogênio A e B, enquanto nas pessoas de sangue tipo O, não se observa aglutinogênio nas hemácias.



